キリンホールディングス株式会社のプレスリリース
GRAS(Generally Recognized As Safe)とは、「一般に安全とみなされている」という意味で、一定の使用目的における条件下での安全性を証明するものです。専門家の知見および経験、科学的データなどに基づいて安全性を証明し、GRAS自己認証(GRAS Determination)を行うことで、その物質を食品の原料として米国内で販売することが可能になります。さらに、事業者が任意でGRAS物質をFDAに通知し、FDAが申請内容に異議を申し立てない場合、その物質は GRAS物質として、FDAが発行する「GRAS Notice Inventory」に掲載されます。
今回、協和発酵バイオはHMO 3品目を育児用ミルクの原材料として販売するにあたり、GRAS自己認証を行い、FDAより当社の安全性判断に異議なしと結論づけたNo question letterを受領し、GRAS通知手続きを完了しました。
協和発酵バイオは、1990年代からHMO研究開発の最前線に立ち、2000年に世界で初めて工業レベルでのHMO大量生産システムを構築し※3、2022年11月には、タイに新設した最先端の工場でHMO 3品目の商業生産を開始しました。今後、新規食品原料の申請が承認された国・地域で、HMOの展開を拡大させていきます。
※1:通知番号はそれぞれ、2FLがGRN 1051、3SLがGRN 1052、6SLがGRN 1053
※2:医学的もしくは食事上の問題を有する乳児に使用する特殊なミルクを除く、乳児用ミルクおよびフォローアップミルク
※3:Tetsuo Endo et. al.,Appl. Microbiol. Biotechnol. 53, 257-261 (2000)
■「ヒトミルクオリゴ糖(HMO)」とは
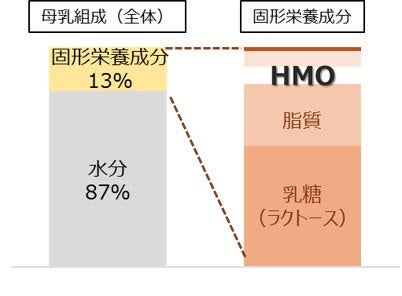
母乳に含まれるオリゴ糖の総称です。母乳中の固形成分の中では、ラクトース、脂質に次ぐ、三番目に多い成分で、これまでに200種類以上のHMOが母乳から発見されています。牛乳や他哺乳類由来の乳にはほとんど含まれず、特にヒトの初乳に多く含まれることから、乳幼児にとって重要な成分であることが知られています。HMO入り粉ミルク市場は欧米で継続的に伸長しているだけでなく、人口増加が見込まれる中国・東南アジア地域でも消費拡大が期待されており、今後の年平均成長率は20%~30%程度※4と予測されています。
※4:Barclays, “HMOs the next frontier of Infant Formula innovation”, March 2022
HMO入り粉ミルク市場の年平均成長率は、2022年~2027年にかけての予測値
■協和発酵バイオ社長 神崎夕紀コメント
私たちは、HMO 3品目に関する GRAS 通知について、FDA から No Question Letter を受領したことを非常に嬉しく思っています。GRAS通知手続きの完了は、乳児用粉ミルクや従来の食品メーカーに安全で革新的なソリューションを提供するという当社のコミットメントを証明するものです。私たちの HMO の導入は、世界中の乳児と消費者に大きな健康利益をもたらすと信じています。
協和発酵バイオは、ライフサイエンスとテクノロジーの進歩を追求し、新しい価値の創造により、世界の人々の健康と豊かさに貢献します。
キリングループは、自然と人を見つめるものづくりで、「食と健康」の新たなよろこびを広げ、こころ豊かな社会の実現に貢献します。


